(круглосуточно)

Приложение 36,6
Двойные бонусы в приложении
Доступность товаров
Форма выпуска
Бренд
Производители
Страна-производитель
Отпуск по рецепту
Цена
Дозировка
Количество (шт.)
Действующее вещество Дапаглифлозин в Мытищах
Фильтры
Цена действует только при заказе на сайте
Доставляем по электронному рецепту
Форсига Таблетки покрытые пленочной оболочкой 10 мг 30 шт
Производитель: AstraZeneca, Россия
Действующее вещество: Дапаглифлозин
Форсига
Доставляем по электронному рецепту
Форсига 10 мг № 90
Производитель: AstraZeneca, Россия
Действующее вещество: Дапаглифлозин
Похожие товары из категории Дапаглифлозин
Доставляем по электронному рецепту
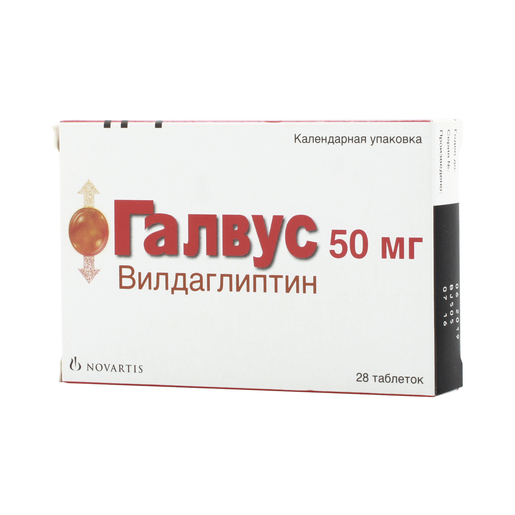
Галвус Таблетки 50 мг 28 шт
Производитель: Новартис Фарма, Россия
Действующее вещество: Вилдаглиптин
Доставляем по электронному рецепту
Галвус Мет Таблетки покрытые пленочной оболочкой 50 мг + 500 мг 30 шт
Производитель: Новартис Фарма, Россия
Действующее вещество: Вилдаглиптин+Метформин
Доставляем по электронному рецепту
Галвус Мет Таблетки покрытые пленочной оболочкой 50 мг + 1000 мг 30 шт
Производитель: Новартис Фарма, Россия
Действующее вещество: Вилдаглиптин+Метформин
Доставляем по электронному рецепту
Галвус Мет Таблетки 50 мг + 850 мг 30 шт
Производитель: Новартис Фарма, Швейцария
Действующее вещество: Вилдаглиптин+Метформин
Инструкция по применению
Показания к применению
Сахарный диабет типа 2 в дополнение к диете и физическим упражнениям для улучшения гликемического контроля в качестве:- монотерапии.- добавления к терапии метформином, производными сульфонилмочевины (в т.ч. в комбинации с метформином), тиазолидиндионами, ингибиторами ДПП-4 (в т.ч. в комбинации с метформином), препаратами инсулина (в т.ч. в комбинации с одним или двумя гипогликемическими ЛС для перорального применения) при отсутствии адекватного гликемического контроля.- стартовой комбинированной терапии с метформином при целесообразности данной терапии.
Фармакологическое действие
гипогликемическоеФармакодинамикаСелективный обратимый ингибитор натрий-глюкозного котранспортера 2-го типа (SGLT2) (константа ингибирования (Кi) - 0,55 нмоля). SGLT2 селективно экспрессируется в почках и не обнаруживается более чем в 70 других тканях организма (в т.ч. в печени, скелетных мышцах, жировой ткани, молочных железах, мочевом пузыре и головном мозге). SGLT2 является основным переносчиком, участвующим в процессе реабсорбции глюкозы в почечных канальцах. Реабсорбция глюкозы в почечных канальцах у пациентов с сахарным диабетом типа 2 продолжается, несмотря на гипергликемию. Тормозя почечный перенос глюкозы, дапаглифлозин снижает ее реабсорбцию в почечных канальцах, что приводит к выведению глюкозы почками. Результатом действия дапаглифлозина является снижение концентрации глюкозы натощак и после приема пищи, а также снижение концентрации гликозилированного Hb у пациентов с сахарным диабетом типа 2.Выведение глюкозы (глюкозурический эффект) наблюдается уже после приема первой дозы, сохраняется в течение последующих 24 ч и продолжается на протяжении всей терапии. Количество глюкозы, выводимой почками за счет этого механизма, зависит от концентрации глюкозы в крови и СКФ. Дапаглифлозин не нарушает нормальную продукцию эндогенной глюкозы в ответ на гипогликемию. Действие дапаглифлозина не зависит от секреции инсулина и чувствительности к инсулину. В клинических исследованиях дапаглифлозина отмечалось улучшение функции бета-клеток (тест НОМА, homeostasis model assessment).Выведение глюкозы почками, вызванное дапаглифлозином, сопровождается потерей калорий и снижением массы тела. Ингибирование дапаглифлозином натрий-глюкозного котранспорта сопровождается слабым диуретическим и транзиторным натрийуретическим эффектом.Дапаглифлозин не оказывает воздействие на другие переносчики глюкозы, осуществляющие транспорт глюкозы к периферическим тканям, и проявляет более чем в 1400 раз большую селективность к SGLT2, чем к SGLT1, основному транспортеру в кишечнике, отвечающему за всасывание глюкозы.После приема дапаглифлозина здоровыми добровольцами и пациентами с сахарным диабетом типа 2наблюдалось увеличение количества выводимой почками глюкозы. При приеме дапаглифлозина в дозе 10 мг/сут в течение 12 нед примерно 70 г глюкозы в сутки выделялось почками (что соответствует 280 ккал/сут). У пациентов с сахарным диабетом типа 2, получавших дапаглифлозин в дозе 10 мг/сут длительно (до 2 лет), выведение глюкозы поддерживалось на протяжении всего курса терапии.Выведение глюкозы почками при применении дапаглифлозина также приводит к осмотическому диурезу и увеличению объема мочи. Увеличение объема мочи у пациентов с сахарным диабетом типа 2, получавших дапаглифлозин в дозе 10 мг/сут, сохранялось в течение 12 нед и составляло примерно 375 мл/сут.Увеличение объема мочи сопровождалось небольшим и транзиторным повышением выведения натрия почками, что не приводило к изменению концентрации натрия в сыворотке крови. Запланированный анализ результатов 13 плацебо-контролируемых исследований продемонстрировал снижение сАД на 3,7 мм рт. ст. и дАД на 1,8 мм рт. ст. на 24-й нед терапии дапаглифлозином в дозе 10 мг/сут по сравнению со снижением сАД и дАД на 0,5 мм рт. ст. в группе плацебо. Аналогичное снижение АД наблюдалось на протяжении 104 нед лечения.При применении дапаглифлозина в дозе 10 мг/сут у пациентов с сахарным диабетом типа 2 с неадекватным контролем гликемии и артериальной гипертензией, получающих блокаторы рецепторов ангиотензина II, ингибиторы АПФ, в т.ч. в комбинации с другими гипотензивными ЛС, было отмечено уменьшение показателя гликозилированного Hb на 3,1% и снижение сАД на 4,3 мм рт. ст. через 12 нед терапии по сравнению с плацебо.ФармакокинетикаАбсорбция. После приема внутрь дапаглифлозин быстро и полностью всасывается в ЖКТ и может приниматься как во время приема пищи, так и вне его. Сmax обычно достигается в течение 2 ч после приема натощак. Значения Сmax и AUC увеличиваются пропорционально дозе дапаглифлозина. Абсолютная биодоступность дапаглифлозина при приеме внутрь в дозе 10 мг составляет 78%. Прием пищи оказывал умеренное влияние на фармакокинетику дапаглифлозина у здоровых добровольцев. Прием пищи с высоким содержанием жиров снижал Сmax дапаглифлозина на 50%, удлинял Тmax примерно на 1 ч, но не влиял на AUC по сравнению с приемом натощак. Эти изменения не являются клинически значимыми.Распределение. Дапаглифлозин примерно на 91% связывается с белками плазмы. У пациентов с различными заболеваниями, например с нарушениями функции почек или печени, этот показатель не изменялся.Метаболизм. Дапаглифлозин — С-связанный гликозид, агликон которого связан с глюкозой углерод-углеродной связью, что обеспечивает его устойчивость в отношении глюкозидаз. Средний Т1/2 у здоровых добровольцев составляет 12,9 ч после однократного приема дапаглифлозина внутрь в дозе 10 мг. Дапаглифлозин метаболизируется с образованием главным образом неактивного метаболита дапаглифлозин-3-О-глюкуронида.После приема внутрь 50 мг 14С-дапаглифлозина 61% принятой дозы метаболизируется в дапаглифлозин-3-О-глюкуронид, на долю которого приходится 42% общей плазменной радиоактивности (по AUC0–12). На долю неизмененного дапаглифлозина приходится 39% общей плазменной радиоактивности. Доли остальных метаболитов по отдельности не превышают 5% общей плазменной радиоактивности. Дапаглифлозин-3-О-глюкуронид и другие метаболиты не оказывают фармакологическое действие. Дапаглифлозин-3-О-глюкуронид формируется под действием фермента уридиндифосфат-глюкуронозилтрансферазы 1А9 (UGT1A9), присутствующего в печени и почках, изоферменты цитохрома CYP вовлечены в метаболизм в меньшей степени.Выведение. Дапаглифлозин и его метаболиты выводятся преимущественно почками и только менее 2% — в неизмененном виде. После приема 50 мг 14С-дапаглифлозина было обнаружено 96% радиоактивности — 75% в моче и 21% — в фекалиях. Примерно 15% радиоактивности, обнаруженной в фекалиях, приходилось на неизмененный дапаглифлозин.Особые группы пациентовНарушение функции почек. В равновесном состоянии (среднее значение AUC) системная экспозиция дапаглифлозина у пациентов с сахарным диабетом типа 2 и почечной недостаточностью легкой, средней или тяжелой степени (определяемой по клиренсу йогексола) была на 32, 60 и 87% выше, чем у больных с сахарным диабетом типа 2 и нормальной функцией почек соответственно. Количество глюкозы, выводимой почками в течение суток при приеме дапаглифлозина в равновесном состоянии, зависело от состояния функции почек. У пациентов с сахарным диабетом типа 2 и нормальной функцией почек, и с почечной недостаточностью легкой, средней или тяжелой степени в сутки выводилось 85, 52, 18 и 11 г глюкозы соответственно. Не выявлено различий в связывании дапаглифлозина с белками плазмы крови у здоровых добровольцев и у пациентов с почечной недостаточностью различной степени тяжести. Неизвестно, оказывает ли гемодиализ влияние на экспозицию дапаглифлозина.Нарушение функции печени. У пациентов с печеночной недостаточностью легкой или средней степени тяжести средние значения Сmax и AUC дапаглифлозина были соответственно на 12 и 36% выше по сравнению со здоровыми добровольцами. Данные различия не являются клинически значимыми, поэтому корректировка дозы дапаглифлозина при печеночной недостаточности легкой и средней степени тяжести не требуется. У пациентов с печеночной недостаточностью тяжелой степени (класс С по шкале Чайлд-Пью) средние значения Сmax и AUC дапаглифлозина были на 40 и 67% выше соответственно по сравнению со здоровыми добровольцами.Пожилой возраст (>65 лет). Не отмечалось клинически значимого увеличения экспозиции у пациентов в возрасте до 70 лет (если не учитывать другие факторы, помимо возраста). Тем не менее, можно ожидать увеличение экспозиции за счет снижения функции почек, связанного с возрастом. Данные об экспозиции у пациентов в возрасте старше 70 лет недостаточны.Пол. У женщин среднее значение AUC в равновесном состоянии на 22% превышает аналогичный показатель у мужчин.Расовая принадлежность. Клинически значимых различий системной экспозиции у представителей европеоидной, негроидной и монголоидной рас не выявлено.Масса тела. Отмечены более низкие значения экспозиции при повышенной массе тела. Поэтому у пациентов с низкой массой тела может отмечаться некоторое повышение экспозиции, а у пациентов с повышенной массой тела — снижение экспозиции дапаглифлозина. Однако данные различия не являются клинически значимыми.
Передозировка
Дапаглифлозин безопасен и хорошо переносится здоровыми добровольцами при однократном приеме в дозах до 500 мг (в 50 раз выше рекомендуемой дозы). Глюкоза определялась в моче после приема (как минимум в течение 5 дней после приема дозы 500 мг), при этом не выявлены случаи обезвоживания, гипотонии, электролитного дисбаланса, клинически значимого влияния на интервал QTc. Частота развития гипогликемии была схожей с частотой при приеме плацебо. В клинических исследованиях у здоровых добровольцев и пациентов с сахарным диабетом типа 2, принимавших дапаглифлозин однократно в дозах до 100 мг (в 10 раз выше максимальной рекомендуемой дозы) в течение 2 нед, частота развития гипогликемии была немного выше, чем при приеме плацебо, и не зависела от дозы. Частота развития нежелательных явлений, включая обезвоживание или артериальную гипотензию, была схожей с частотой в группе плацебо, при этом не выявлено клинически значимых, дозозависимых изменений лабораторных показателей, включая сывороточную концентрацию электролитов и биомаркеров функции почек.В случае передозировки необходимо проводить поддерживающую терапию, учитывая состояние больного. Выведение дапаглифлозина с помощью гемодиализа не изучалось.
Противопоказания
Повышенная индивидуальная чувствительность к дапаглифлозину. сахарный диабет типа 1. диабетический кетоацидоз. почечная недостаточность средней и тяжелой степени (СКФ <60 мл/мин/1,73 м2) или терминальная стадия почечной недостаточности. беременность и период грудного вскармливания. возраст до 18 лет (безопасность и эффективность не изучены). пациенты, получающие петлевые диуретики (см. «Взаимодействие»), или со сниженным ОЦК, например вследствие острых заболеваний (таких как желудочно-кишечные). пожилые пациенты в возрасте 75 лет и старше (для начала терапии).
Применение при беременности и кормлении грудью
Категория действия на плод по FDA — C.Дапаглифлозин противопоказан в период беременности (применение в период беременности не изучено). В случае диагностирования беременности терапия дапаглифлозином должна быть прекращена.Неизвестно, проникает ли дапаглифлозин и/или его неактивные метаболиты в грудное молоко. Нельзя исключить риск для новорожденных/младенцев. Дапаглифлозин противопоказан в период грудного вскармливания.
Источники
- Государственный реестр лекарственных средств;
- Международная классификация болезней (МКБ-10);
- Официальная информация от производителя.
Проверено специалистом
Чепурнова Наталья Александровна
Фармацевт, стаж 10 лет